Guillermo López Lluch, Universidad Pablo de Olavide
Nuestras células no tienen nada que envidiarle a las máquinas más sofisticadas que haya construido el ser humano. Están divididas en compartimentos –que llamamos orgánulos– que cumplen a rajatabla con las diferentes funciones que tienen asignadas: producir energía, fabricar y modificar proteínas, digerir sustancias externas, transportar sustancias o controlar la expresión del genoma entre otras.
En este reparto de tareas, las encargadas de producir la energía son las mitocondrias. Que además son esenciales para generar y modificar componentes celulares, regular la señalización celular o determinar la vida o la muerte de la propia célula.
Para entender hasta que punto son importantes basta saber que enfermedades como el síndrome metabólico, la obesidad, la hipertensión, la diabetes tipo 2, las enfermedades cardiovasculares, el alzhéimer y párkinson están asociadas a la acumulación de mitocondrias deficientes en prácticamente todas las células, tejidos y órganos. Y lo mismo sucede con el envejecimiento.
Las mitocondrias del sistema inmune se dañan
El deterioro mitocondrial no deja indiferente al sistema inmune. Que, dicho sea de paso, es bastante complejo. A grandes rasgos podemos decir que consta de dos subsistemas interconectados: uno que actúa de forma inmediata y otro que se adapta, que aprende y que necesita un periodo de aprendizaje para actuar.
Al primero lo conocemos como sistema innato. Está formado por células como los macrófagos, los neutrófilos o las células asesinas, además del sistema del complemento y de proteínas como el interferón.
Al segundo lo denominamos sistema adaptativo y está formado por linfocitos B, que producen anticuerpos, y linfocitos T. Estos últimos tienen sus propias patrullas: unas que coordinan la respuesta del sistema inmunitario (linfocitos T ayudantes o Th) y otras dedicadas a eliminar células infectadas por virus, tumorales o simplemente dañadas (linfocitos T citotóxicos o Tc).
La presencia de mitocondrias dañadas afecta a casi todas estas células del sistema inmunitario y es un factor clave en su deficiente funcionamiento durante el envejecimiento (inmunosenescencia) y en la generación y mantenimiento de un estado de inflamación crónica conocido como inflamm-aging.
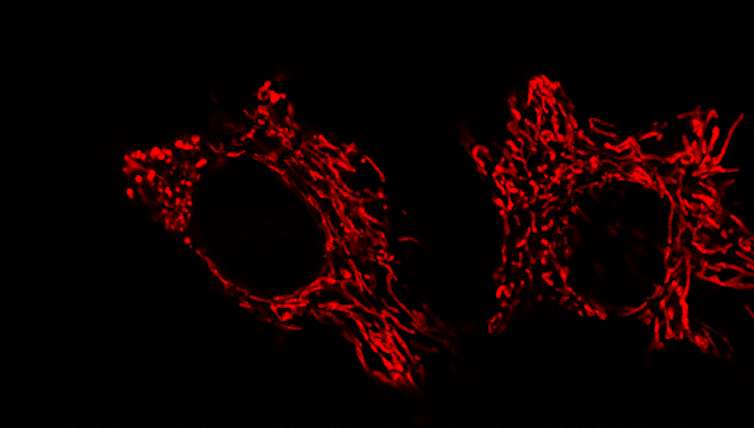
¿Afectan las mitocondrias a la respuesta frente a virus?
Para responder a esta pregunta hay que empezar por entender que, cuando los macrófagos detectan virus, producen y liberan una serie de proteínas conocidas como citoquinas capaces de generar una respuesta inflamatoria. En enfermedades como la obesidad o la diabetes o en el envejecimiento, las mitocondrias deficientes mantienen a los macrófagos en un estado preactivado dando lugar a un estado inflamatorio crónico.
¿Y qué ocurre ante un ataque viral? Pues que los macrófagos lanzan una respuesta inflamatoria más agresiva de lo normal conocida como tormenta de citoquinas. Esta tormenta se considera un factor de gravedad en la COVID-19 que puede generar un fallo multiorgánico, incluso la muerte. Es más, se sospecha que es la causa de las múltiples secuelas que provoca esta enfermedad, sobre todo de las que afectan al sistema circulatorio y al cerebro.
Por otro lado, los macrófagos y las células infectadas por el virus fabrican también interferón. Esta molécula cumple una doble función. De un lado, hace que las células vecinas reduzcan su actividad para que no se puedan fabricar nuevas partículas víricas a partir de ellas. Simultáneamente, el interferón alerta a los linfocitos T y a los linfocitos B (productores de anticuerpos) para que inicien el contraataque.
¿Y qué tiene que ver todo esto con las mitocondrias? Resulta que la producción de interferón depende de una serie de señales dentro de las células en las que las mitocondrias están muy implicadas. Si las mitocondrias están dañadas, estas señales no se producen y la liberación de interferón se reduce . Eso permite al virus replicarse más activamente.
Se sospecha que si los pacientes más graves de COVID-19 presentan bajos niveles de interferón es debido a la deficiencia mitocondrial y a la actividad bloqueante del virus. Además, los linfocitos también necesitan mitocondrias sanas para cumplir con su función de manera rápida y eficiente.
De lo anterior se deduce que la respuesta inmunitaria frente a infecciones víricas, ya sea el SARS-CoV-2 o el virus de la gripe, requiere de unas células del sistema inmunitario con mitocondrias sanas. Mantener nuestras mitocondrias sanas con una dieta equilibrada y rica en vegetales, como la dieta mediterránea, y manteniendo actividad física continua y moderada, es esencial para defendernos frente a virus y patógenos en general de manera rápida, contundente y eficaz.![]()
Guillermo López Lluch, Catedrático del área de Biología Celular. Investigador asociado del Centro Andaluz de Biología del Desarrollo. Investigador en metabolismo, envejecimiento y sistemas inmunológicos y antioxidantes., Universidad Pablo de Olavide
Este artículo fue publicado originalmente en The Conversation. Lea el original.
![]()









































