
Las enfermedades mitocondriales representan uno de los grupos más comunes de enfermedades genéticas. Con una prevalencia superior a 1 en 5000 adultos, la mayoría de ellas todavía carecen de un tratamiento eficaz. Las terapias actuales son puramente paliativas y, en la mayoría de los casos, insuficientes, de ahí que la comunidad científica deba desarrollar nuevos enfoques para compensar y, si es posible, revertir la disfunción mitocondrial. En esta línea trabaja el equipo científico de la Universidad Pablo de Olavide, dirigido por el profesor José Antonio Sánchez-Alcázar, que ha publicado recientemente un estudio que demuestra cómo las alteraciones patológicas en la mutación mitocondrial GFM1 pueden ser corregidas por activadores de la UPR, dando un paso adelante en la estrategia terapéutica para las enfermedades mitocondriales.
En el estudio, el grupo del doctor Sánchez Alcázar abordó el problema utilizando como modelo biológico los fibroblastos de un paciente portador de una mutación en el gen GFM1, que está implicado en la síntesis de proteínas mitocondriales. “La mutación GFM1 causa deficiencias de la cadena respiratoria y cuadros clínicos muy graves. Los fibroblastos GFM1 mutantes no pueden sobrevivir en un medio con galactosa que fuerza a las células a depender exclusivamente de la función mitocondrial”, explican los investigadores. “Sin embargo, el tratamiento con tetraciclina permitió la supervivencia de los fibroblastos GFM1 mutantes en este medio”, añaden.
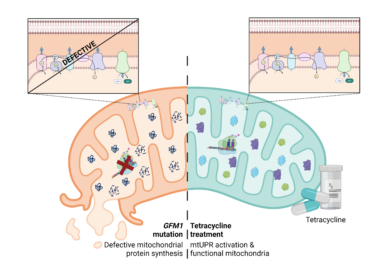
Con este trabajo, los investigadores e investigadoras de la UPO demuestran que la tetraciclina activa la respuesta a proteínas mal plegadas mitocondrial (UPRmt), una vía compensatoria que regula el correcto funcionamiento mitocondrial. Además, comprobaron que la activación de UPRmt mejora la bioenergética celular de las células mutantes y restaura parcialmente la expresión de las proteínas mitocondriales. Los resultados fueron confirmados en neuronas inducidas obtenidas por reprogramación directa de los fibroblastos del paciente.
“El estudio propone que la activación de los mecanismos compensatorios celulares como la UPRmt es una estrategia terapéutica prometedora para las enfermedades mitocondriales”, afirman.
Plataforma MITOCURE: Medicina de precisión personalizada en las enfermedades mitocondriales
Las enfermedades mitocondriales abarcan un amplio espectro de trastornos musculares y neurodegenerativos, crónicos y progresivos, causadas por mutaciones en el ADN nuclear (nDNA) o mitocondrial (mtDNA), la mayoría de las cuales no tienen tratamiento eficaz. Estas enfermedades tienen una gran heterogeneidad y afectan fundamentalmente a la capacidad de producción energética de las células.
Las terapias farmacológicas actuales se basan fundamentalmente en: 1) Eliminar los metabolitos tóxicos; 2) Intentar circunvalar los bloqueos de la cadena respiratoria; 3) Administrar metabolitos y cofactores para mejorar la síntesis de ATP; 4) Prevenir el estrés oxidativo.
Dada la diversidad de mutaciones y las diferentes opciones terapéuticas, la propuesta de MITOCURE defiende que en las enfermedades mitocondriales es obligado una aproximación terapéutica personalizada.
Con esta plataforma los investigadores e investigadoras de la UPO evalúan la efectividad terapéutica de los distintos tratamientos disponibles en los fibroblastos derivados de los pacientes mitocondriales y en las células neuronales generadas por reprogramación directa. Para conseguir este objetivo, estudian los efectos de estos tratamientos sobre las alteraciones fisiopatológicas presentes en los fibroblastos y células neuronales derivadas de los pacientes de una manera personalizada.
En los modelos celulares estudian la proliferación celular y/o muerte celular en medio con galactosa (que fuerza la obtención de energía por la mitocondria), las actividades enzimáticas de la cadena respiratoria mitocondrial, los niveles de expresión de las proteínas mitocondriales, el potencial de membrana mitocondrial, y la activación de la degradación de las mitocondrias y/o la apoptosis.
En la actualidad, la plataforma MITOCURE está realizando medición de precisión personalizada en más de 30 mutaciones que afectan directa o indirectamente a la formación de energía por las mitocondrias.
Artículo de referencia:
UPRmt activation improves pathological alterations in cellular models of mitochondrial diseases.
Juan M. Suárez-Rivero, Carmen J. Pastor-Maldonado, Suleva Povea-Cabello, Mónica Álvarez-Córdoba, Irene Villalón-García, Marta Talaverón-Rey, Alejandra Suárez-Carrillo, Manuel Munuera-Cabeza, Diana Reche-López, Paula Cilleros-Holgado, Rocío Piñero-Perez and José A. Sánchez-Alcázar
Orphanet Journal of Rare Diseases, 17:204, 2022
DOI: https://doi.org/10.1186/s13023-022-02331-8
Referencias del grupo de investigación:
https://sanchezalcazarlab.com/
https://pubmed.ncbi.nlm.nih.gov/?term=sanchez+alcazar&sort=pubdate
https://www.researchgate.net/profile/Jose-Sanchez-Alcazar



































